作者:汪晶晶
导读:
光镊——一种利用光捕获与操控微小物体的工具。2018年,这项 “爆冷”的技术夺得诺贝尔物理学奖的桂冠,也终于实现了“光捕获之父” Arthur Ashkin的预言:“我想生物学领域可能会因为用光镊做出的伟大工作而获得一次诺贝尔奖。”本期将从光镊在生物学领域的应用发展方面做一概述。
一、光镊的由来
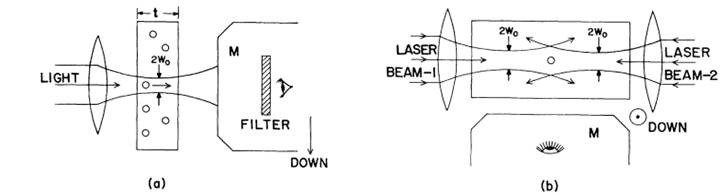

二、光镊在生物学领域的应用与发展
光镊在生物学领域有广泛应用。一个重要的原因是它为生物学家提供了一只“微观手”去操控生物体,像光学显微镜技术一样具有低侵入性。另外,光镊可获得的长度、时间和力学尺度在生物学上从单细胞到单分子水平是具有相关性的。
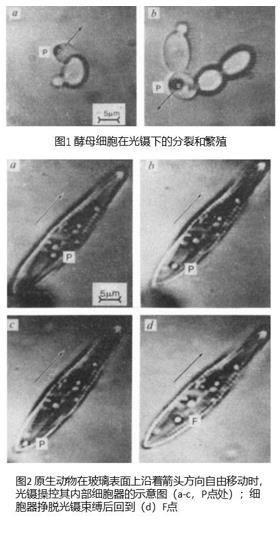
90年代初期,光镊的使用已扩展到单个生物分子水平。在这些单分子研究中,感兴趣的生物分子本身并不是直接被捕获的,而是被光学捕获的微球所操纵,这些微球起着手柄和力传感器的作用(图3)。这种单分子研究的很大一部分包括对单个驱动蛋白活动的研究(Svoboda,Schmidt et al. 1993;Yin,Wang et al. 1995)。这些蛋白移动产生的力和运动可以通过光镊进行研究和控制,用以揭示它们的动力学和能量学特征。
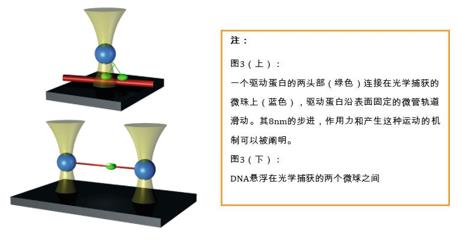
另一个重要的研究领域是DNA。在这些研究中,DNA分子粘附于一个或多个光捕获的小球上,这使得分子可以被拉伸,并通过力学谱研究它们的机械特性(Smith,Cui et al. 1996;Bustamante,Bryant et al. 2003)(图4)。
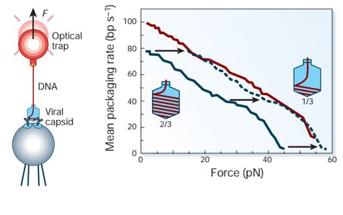
图4 噬菌体DNA的组装
当DNA被噬菌体Ø29马达拉入以填充病毒衣壳时,外部DNA的延伸变短。当衣壳被填充三分之二(蓝色实线)时,组装的力-速度曲线必须偏移约15pN(蓝色虚线),才与衣壳被填充三分之一(红色)时的曲线相符。提示在DNA组装过程中存在因DNA高度压缩而形成的其他内力(将DNA注入宿主细胞的驱动力)。
另外,这些设计被用来研究蛋白与DNA蛋白之间的相互作用(Davenport,Wuite et al. 2000;Dame,Noom et al. 2006;Neupane,Foster et al. 2016)。许多DNA与蛋白之间的相互作用影响DNA的结构,从而影响DNA分子的长度(力学依赖性)。利用光镊,这些长度变化可以通过测量微球的位移来观察(图5)。例如DNA-结合蛋白以及DNA和RNA聚合酶活性的研究。
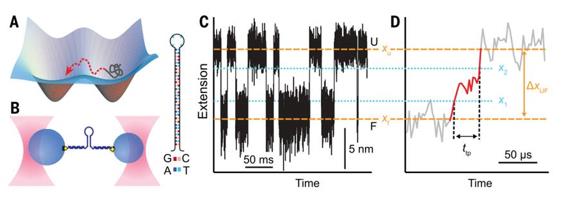
A. 过渡态路径(transition paths)代表蛋白质折叠过程中跨越能量障碍的短暂过程(红线);与之形成对比的是大部分时间在势阱中波动的过程(灰色线)
B. DNA发夹连接在两段“手链”结构上,分别附着在光捕获的两个微球上
C. 恒力状态下,发夹结构在折叠和去折叠状态间维持着动态变化
D.过渡路径(红线):在U(unfolding)和F(folding)之间移动的轨迹
在过去十年中,光镊与其他技术的结合进一步扩大了光镊在生物学领域的影响。包括与多通道微流控系统的结合(Brewer andBianco 2008),不仅提高了实验通量,还提供了更复杂的多步生物学反应过程的原位控制。最引人注目的是,光镊与丰富多样的荧光技术相结合,使得光镊的分析范畴远远超过了机械测量(Heller, Sitterset al. 2013;Block, Witt etal. 2017)(图6)。
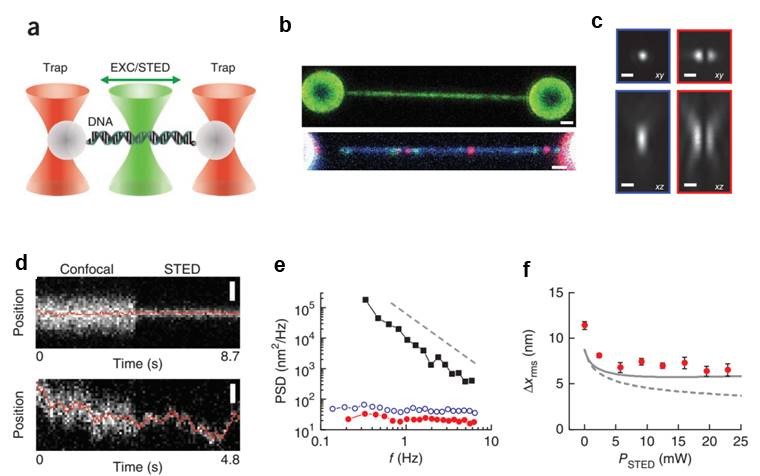
图6 光镊与共聚焦和STED荧光显微镜相结合,可视化单个DNA结合蛋白在DNA上的移动轨迹
a. DNA两端连在两个光镊捕获的微球之间,在DNA上扫描的激发光束(EXC)和叠加的STED光束显示为绿色。b. λDNA和3.2-µm微球的共聚焦荧光图像。c. 共聚焦和1D STED激光束示意图(左侧:共聚焦图像;右侧:STED图像;scale bar:500nm)。d. 光学拉伸DNA上的Atto 647n标记蛋白波动曲线(部分共聚焦,部分STED)。e. 功率谱密度(PSD): 跟踪蛋白质在DNA上的位置。f. 定位精度∆Xrms 与PSTED的函数关系图。
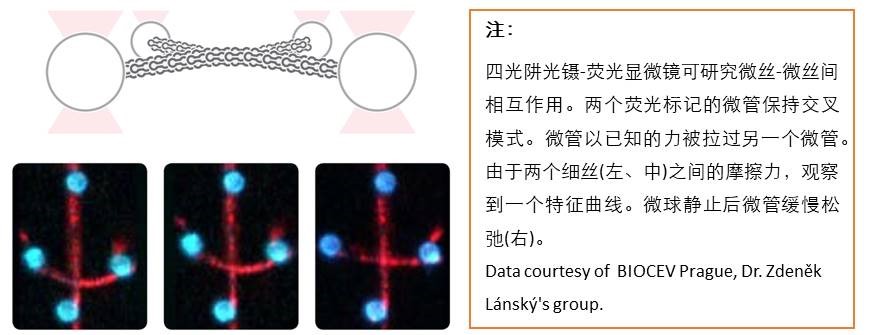
随着近年来商业化光镊系统的出现,这种强大的单分子技术正趋于成熟,为越来越多的生物科学家所使用。随着商业化荧光技术和原子力显微镜(AFM)技术的发展,可以预期商业化光镊将极大地促进我们在单分子水平上的生物学认识。
诺贝尔奖得主朱棣文(Steven Chu)曾在《Physics Today》中说过,“如果在未来十年,另一个诺贝尔奖得主是源于他通过光镊或其他单分子技术在分子生物学领域有了突破性发现,他不会感到惊讶。”(文末附参考文献)

本期参考文献
1. Ashkin, A. (1970)."Acceleration and Trapping of Particles by Radiation Pressure." PhysicalReview Letters 24(4): 156-159.
2. Ashkin, A. and J. M. Dziedzic (1987). "Optical trapping and manipulation of viruses and bacteria." Science(New York, N.Y.) 235(4795):1517-1520.
3. Ashkin, A., J. M. Dziedzic, J. E.Bjorkholm and S. Chu (1986). "Observation of a single-beam gradient forceoptical trap for dielectric particles." Opt Lett 11(5): 288.
4. Ashkin, A., J. M. Dziedzic and T.Yamane (1987). "Optical trapping and manipulation of single cells usinginfrared laser beams." Nature 330(6150):769-771.
5. Block, J., H. Witt, A. Candelli,E. J. G. Peterman, G. J. L. Wuite, A. Janshoff and S. Köster (2017)."Nonlinear Loading-Rate-Dependent Force Response of Individual VimentinIntermediate Filaments to Applied Strain." Physical review letters 118(4): 048101-048101.
6. Brewer, L. R. and P. R. Bianco(2008). "Laminar flow cells for single-molecule studies of DNA-proteininteractions." Nature methods 5(6):517-525.
7. Bustamante, C., Z. Bryant and S.B. Smith (2003). "Ten years of tension: single-molecule DNAmechanics." Nature 421(6921):423-427.
8. Chu, S. (1991). "Lasermanipulation of atoms and particles." Science 253(5022): 861-866.
9. Dame, R. T., M. C. Noom and G. J.L. Wuite (2006). "Bacterial chromatin organization by H-NS proteinunravelled using dual DNA manipulation." Nature 444(7117): 387-390.
10. Davenport, R. J., G. J. Wuite, R.Landick and C. Bustamante (2000). "Single-molecule study oftranscriptional pausing and arrest by E. coli RNA polymerase." Science(New York, N.Y.) 287(5462):2497-2500.
11. Heller, I., G. Sitters, O. D.Broekmans, G. Farge, C. Menges, W. Wende, S. W. Hell, E. J. G. Peterman and G.J. L. Wuite (2013). "STED nanoscopy combined with optical tweezers revealsprotein dynamics on densely covered DNA." Nature methods 10(9): 910-916.
12. Lin, H. Y., N. Fujita, K. Endo,M. Morita, T. Takeda, T. Nakagawa and R. Nishimura (2017). "Isolation andCharacterization of Multipotent Mesenchymal Stem Cells Adhering to Adipocytesin Canine Bone Marrow." Stem Cells Dev 26(6): 431-440.
13. Neupane, K., D. A. N. Foster, D.R. Dee, H. Yu, F. Wang and M. T. Woodside (2016). "Direct observation oftransition paths during the folding of proteins and nucleic acids." Science(New York, N.Y.) 352(6282):239-242.
14. Smith, S. B., Y. Cui and C.Bustamante (1996). "Overstretching B-DNA: the elastic response ofindividual double-stranded and single-stranded DNA molecules." Science(New York, N.Y.) 271(5250):795-799.
15. Svoboda, K., C. F. Schmidt, B. J.Schnapp and S. M. Block (1993). "Direct observation of kinesin stepping byoptical trapping interferometry." Nature 365(6448): 721-727.
16. Yin, H., M. D. Wang, K. Svoboda,R. Landick, S. M. Block and J. Gelles (1995). "Transcription against anapplied force." Science (New York, N.Y.) 270(5242): 1653-1657.
本文章版权归清华大学生物医学测试中心细胞生物学平台所有





