研究背景
生物医药研发中,精准表征复杂生物样品的物理化学性质是质量控制和功能评估的关键。然而,外泌体、糖蛋白等生物大分子体系因其异质性高、结构复杂,传统表征技术往往面临准确性不足、需多种方法交叉验证等挑战。
近期,清华大学蛋白质研究技术中心/生物结构前沿研究中心/膜生物学国家重点实验室李文奇团队与中国食品药品检定研究院生物制品检定所合作,在分析超速离心(Analytical Ultracentrifugation, AUC)技术的创新应用上取得重要进展,为生物制品的质量评价提供了新的技术方案。相关成果“Quantification of Glycan in Glycoproteins via AUCAgent-Enhanced Analytical Ultracentrifugation”、“Comparative analysis of different biophysical techniques for exosome characterization”分别发表在Pharmaceuticals 和Scientific Reports期刊上。
一、糖蛋白定量难题:AUC双信号检测法精准测量多糖/蛋白占比
糖蛋白,这类由蛋白质和糖链组成的生物分子,广泛存在于生物体中,参与细胞识别、信号转导和免疫应答等关键过程。然而,糖基化修饰的高度异质性使得其精确分析极具挑战性。传统的分子量测定方法,如SDS-PAGE、质谱(LC-MS)等,在处理高度糖基化的样品时,常面临分子量被高估、信号复杂难以解析等技术瓶颈。
在“Quantification of Glycan in Glycoproteins via AUCAgent-Enhanced Analytical Ultracentrifugation”研究中,李文奇团队利用分析超速离心技术(AUC)的紫外-可见光与干涉双检测系统,同步捕获样品的沉降信号。基于这一原理,团队在自主开发的AUC分析软件AUCAgent (https://www.frcbs.tsinghua.edu.cn/download/software/133)中建立了全新的糖蛋白分析模型方法,能够在天然溶液中直接计算出糖蛋白中多糖组分的质量分数。
研究团队以带有7个N-糖基化位点的ERBB-2蛋白为模型,对该方法进行了严谨验证。结果显示,与传统方法相比,AUC新方法展现出显著技术优势:
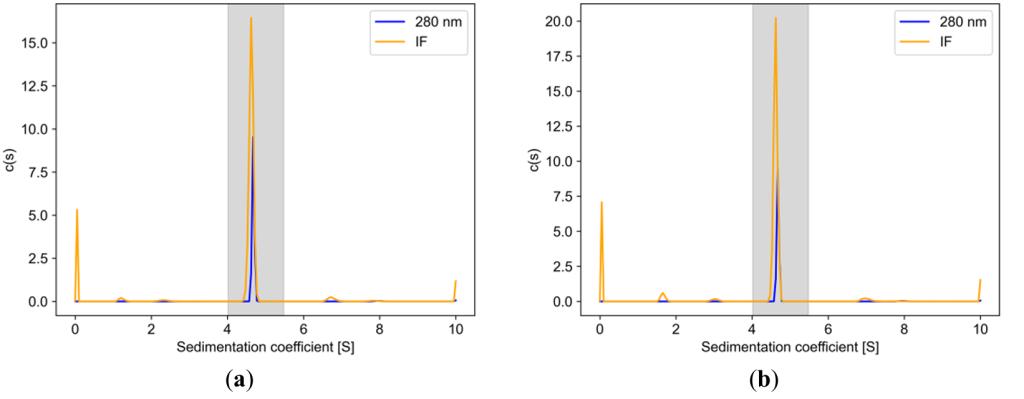
图1: SEDFIT 软件分析得到的蛋白在紫外-可见光(280nm)和干涉信号的c(s) 分布
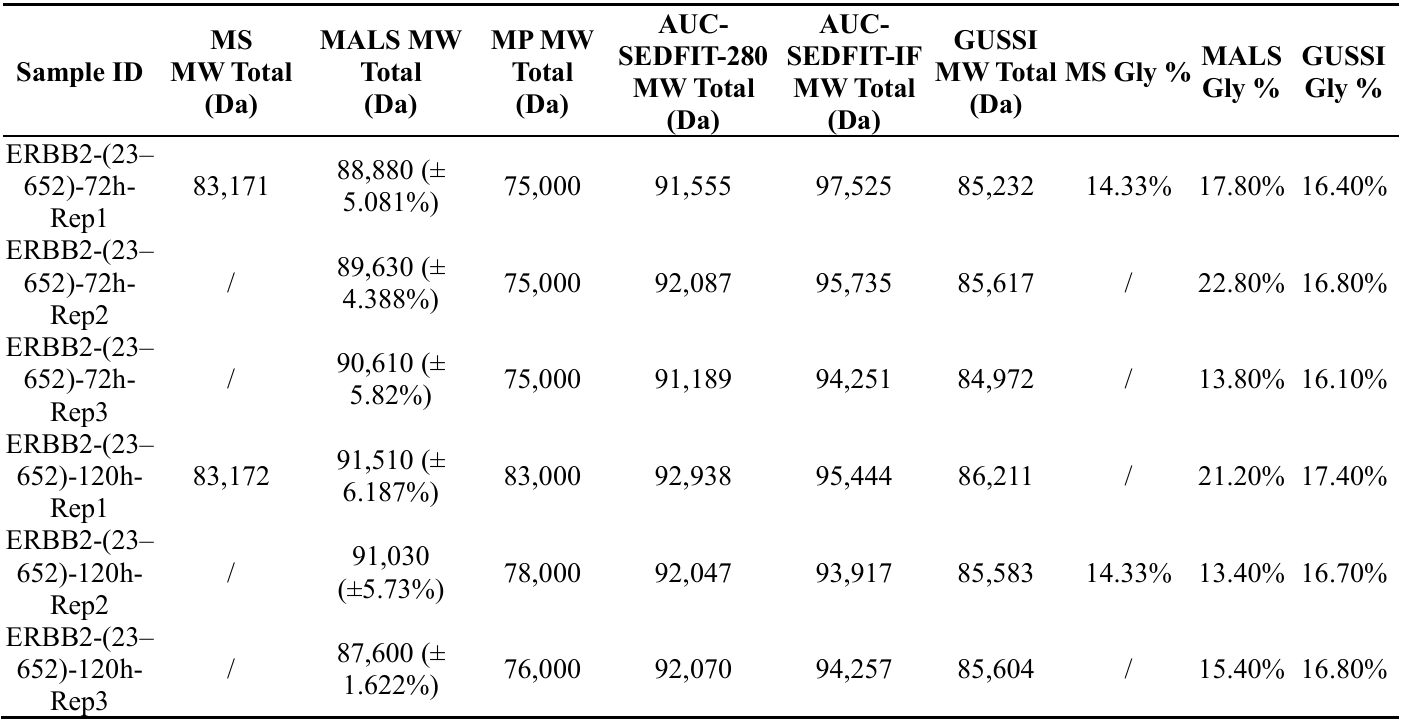
表1: 总蛋白分子量和多糖含量的质谱(MS)、多角度光散射(MALS)、质量光度法(MP)和分析超速离心(AUC)的结果。
高稳定性与重现性: 与常用的SEC-MALS方法相比,新开发的AUC吸光度-干涉法在重复实验中展现出较好的重复性,稳定性更优。研究中作为对比的另一种AUC分析方法(GUSSI软件的糖蛋白分析模块)也显示出极高的稳定性。该方法是一种绝对测量技术,无需如质谱法那样依赖复杂的算法解卷积,也无需像质量光度法(MP)那样使用非糖基化标准品(如BSA)进行校准,有效避免了由上述操作带来的系统误差。
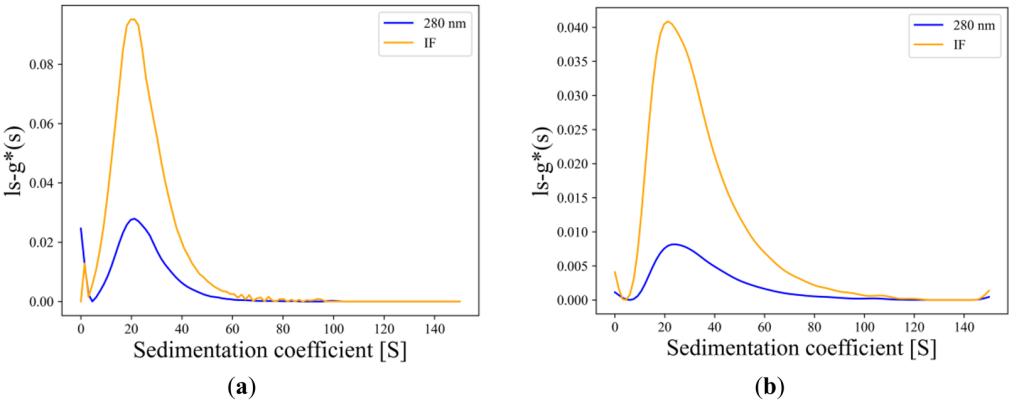
图2: AUCAgent软件分析多糖结合疫苗。a和b 为两种疫苗的沉降系数分布图,显示出样品的多分散性。
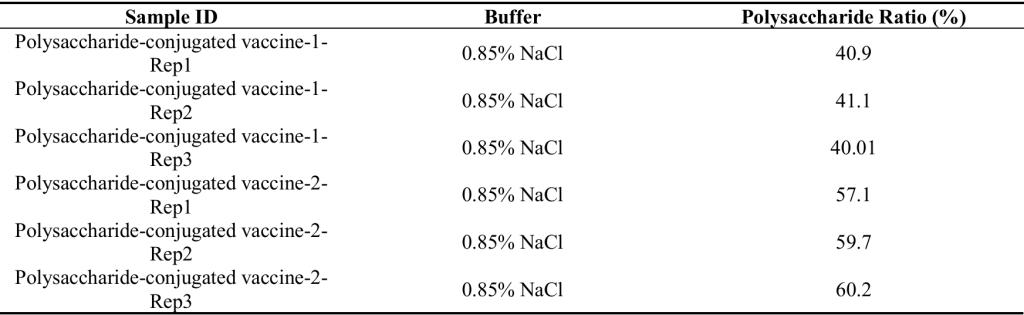
表2: AUCAgent对两种疫苗多糖比例的重复测定结果,展现出良好的重复性。
研究团队进一步将该方法应用于肺炎球菌多糖结合疫苗的分析。而多糖与蛋白载体的比例是这类疫苗的质量控制核心指标之一。实验结果表明,AUCAgent软件能够基于AUC双信号数据,精准计算出疫苗样品中的多糖比例,且三次重复实验的结果高度一致(图2,表2),AUC双信号检测方法也因此显示出其在评估疫苗批次间一致性方面的巨大应用潜力。
二、 多技术正交验证表征外泌体
外泌体作为细胞间通讯的关键信使,在药物递送领域展现出巨大潜力。但外泌体粒径范围为30-150 nm、具有高异质性,纯化样本中还会残留蛋白、脂蛋白等杂质,使得单一表征技术难以全面、可靠地反映其物理化学性质。传统动态光散射(DLS)对少量大颗粒杂质极为敏感,纳米颗粒追踪分析(NTA)技术易受光学干扰,而电阻脉冲传感(RPS)技术则受限于检测下限。如何实现外泌体粒径、浓度与纯度的同步、精准表征,成为制约其质量控制的核心瓶颈之一。
在 “Comparative analysis of different biophysical techniques for exosome characterization”研究中,作者系统比较了DLS、NTA、NanoCoulter与AUC四种技术在牛奶和尿液来源外泌体表征中的表现,首次证实了AUC技术在评估外泌体纯度方面的独特优势,并提出多技术正交验证是建立可靠外泌体表征体系的必要方法。
研究团队采用超速离心法和EXODUS全自动提取系统两种方法分别纯化牛奶和尿液外泌体,随后利用DLS、NTA、NanoCoulter以及SV-AUC(沉降速率-分析超速离心)技术进行不同纯化条件下外泌体的表征,观察并分析各种技术在外泌体表征的差异。
研究结果显示:
DLS技术:速度快,但易受大颗粒干扰,检测结果的重复性差(图3)。
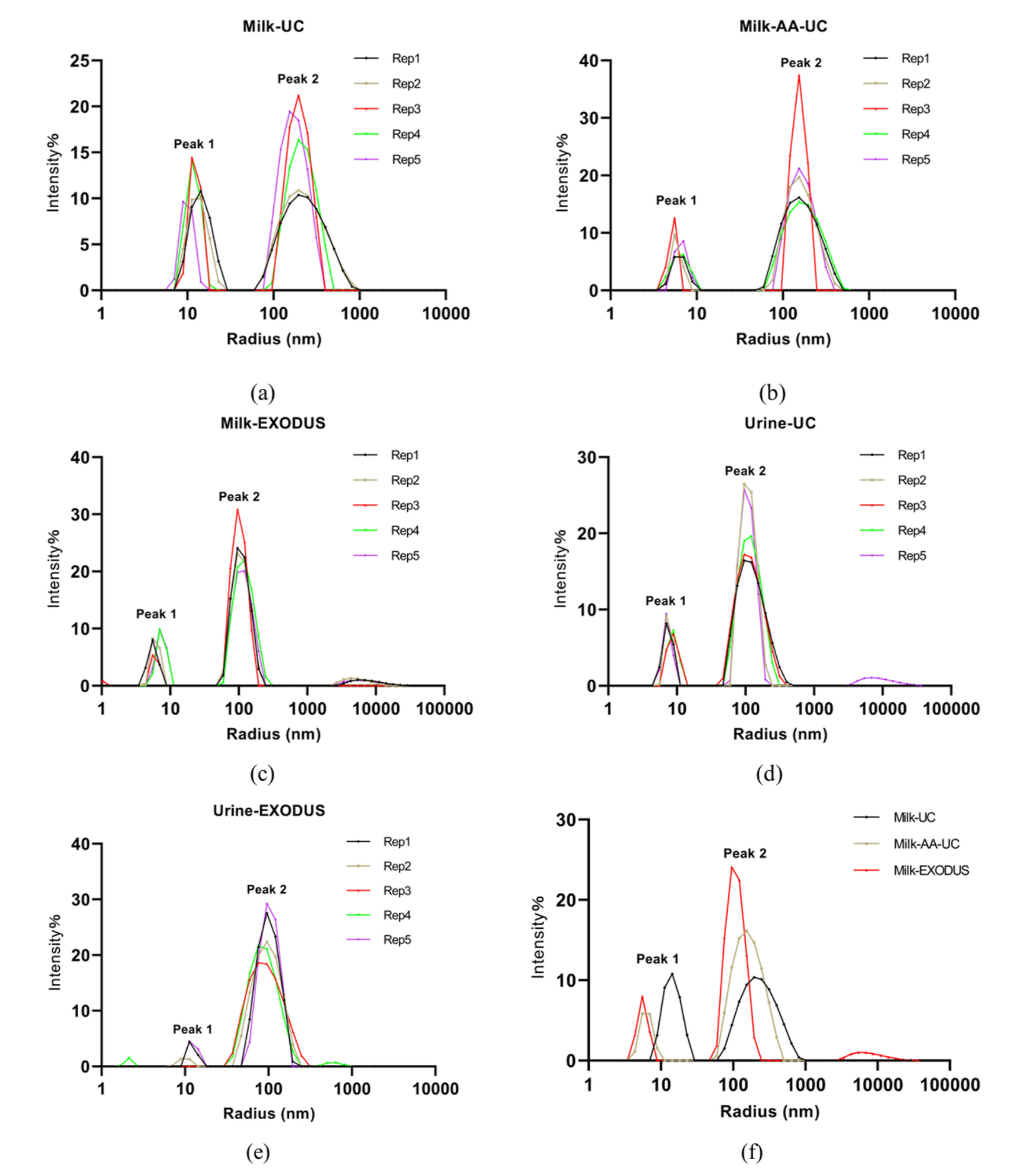
图3: 超速离心法(UC)和EXODUS系统纯化的牛奶及尿液外泌体的动态光散射(DLS)结果:(a)Milk-UC的DLS结果;(b)Milk-AA-UC(超速离心-醋酸沉淀法)的DLS结果;(c)Milk-EXODUS的DLS结果;(d)Urine-UC的DLS结果;(e)Urine-EXODUS的DLS结果。(f)通过UC、AA-UC和EXODUS系统提取的外泌体的DLS结果比较。
NTA技术:分辨率优于DLS,可反映冻融导致的聚集现象,但测得的平均粒径普遍偏大(如Milk-UC为202.1 nm),检测结果也易受杂质影响(图4)。
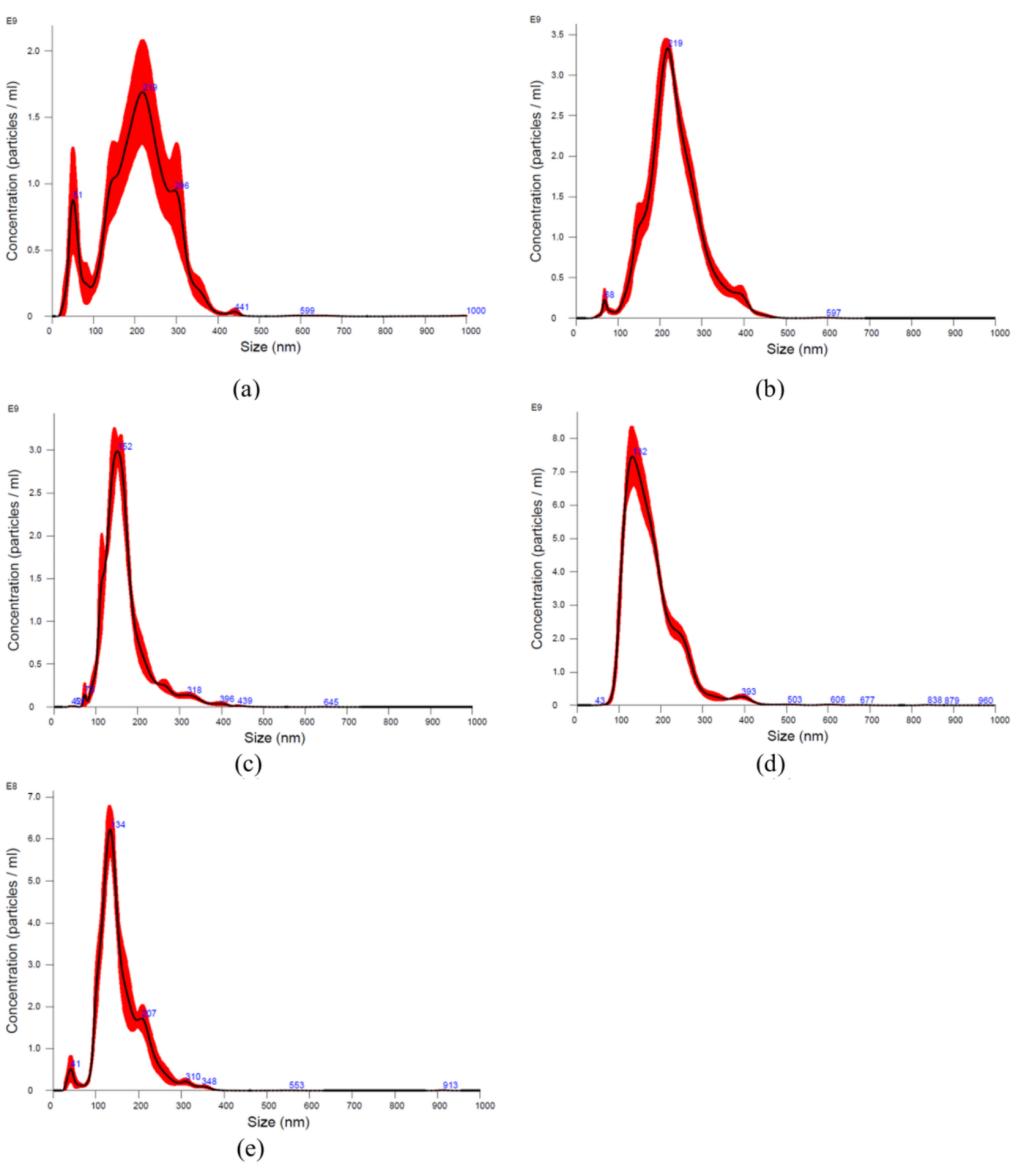
图4:超速离心法(UC)和EXODUS系统纯化的牛奶及尿液外泌体的纳米颗粒追踪分析(NTA)结果:(a)Milk-UC的NTA结果;(b)Milk-AA-UC的NTA结果;(c)Milk-EXODUS的NTA结果;(d)Urine-UC的NTA结果;(e)Urine-EXODUS的NTA结果。
NanoCoulter技术:基于非光学原理,给出的粒径结果(如Milk-UC为92 nm)最接近透射电镜结果,并能提供绝对浓度;但该技术的检测下限受限于选择的纳米孔芯片规格限制,会漏检更小的蛋白杂质,且对冻融造成的变化不敏感(图5)。
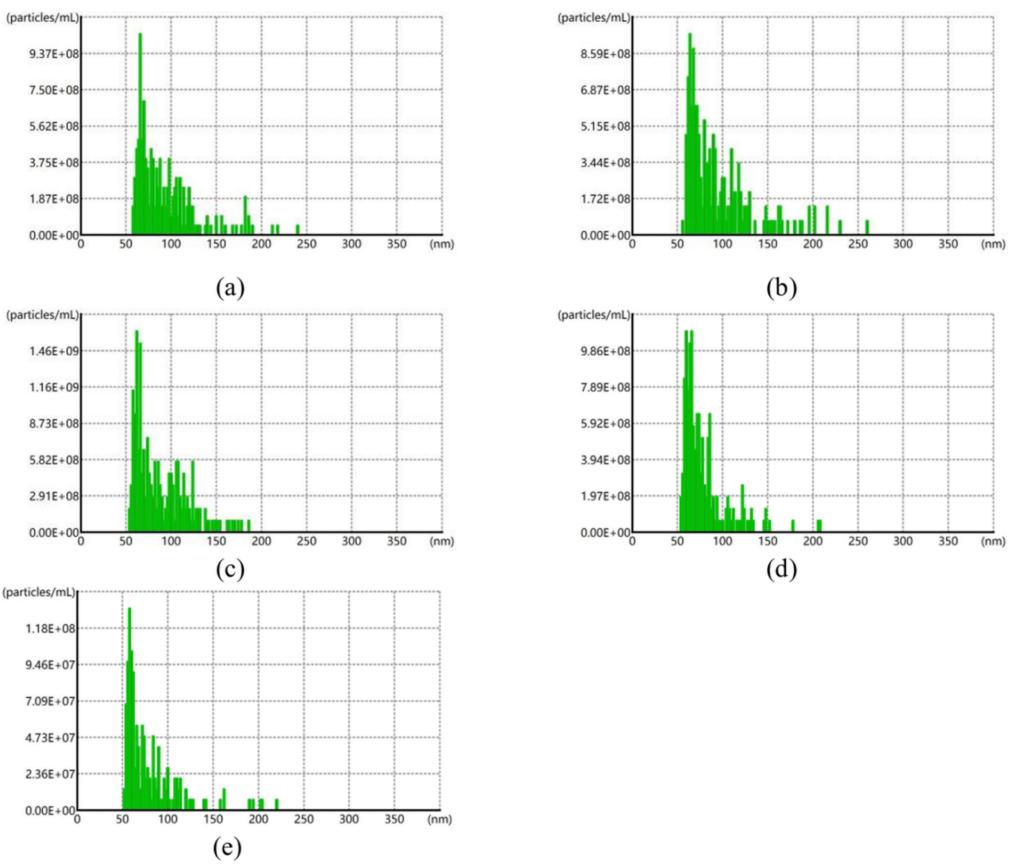
图5. 超速离心法(UC)和EXODUS系统纯化的牛奶及尿液外泌体的NanoCoulter结果:(a)Milk-UC的NanoCoulter结果;(b)Milk-AA-UC的NanoCoulter结果;(c)Milk-EXODUS的NanoCoulter结果;(d)Urine-UC的NanoCoulter结果;(e)Urine-EXODUS的NanoCoulter结果。
AUC技术:虽目前无法直接输出外泌体的粒径分布数据,但可通过沉降图谱与双波长吸收比值,精准评估样本纯度(图6),这是其他三种技术所不具备的。
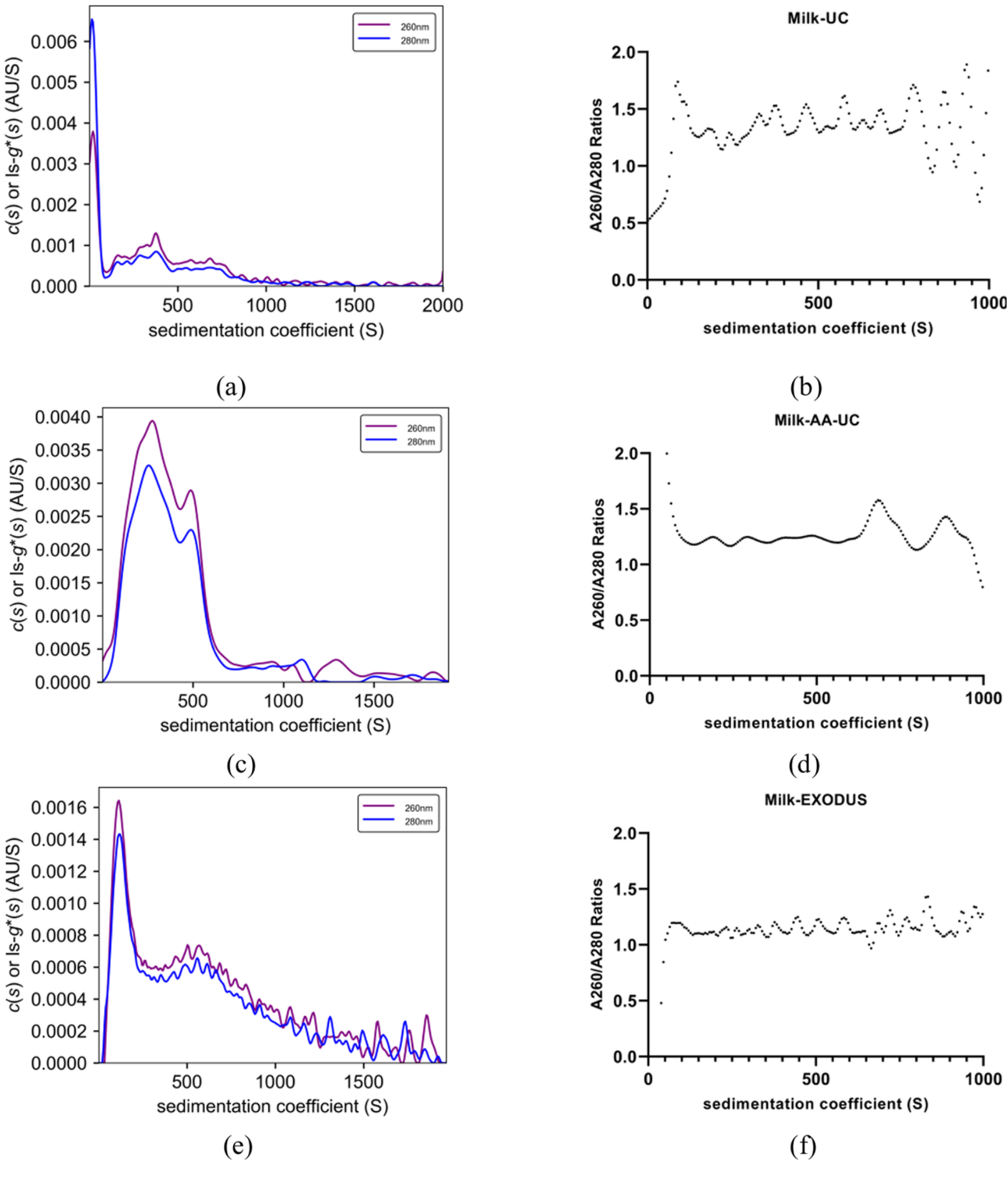
图6:不同方法纯化的牛奶外泌体的沉降速度-分析超速离心(SV-AUC)分析:(a)Milk-UC的ls-g*(s)分布结果;(b)Milk-UC的A260/A280比值;(c)Milk-AA-UC的ls-g*(s)分布结果;(d)Milk-AA-UC的A260/A280比值;(e)Milk-EXODUS的ls-g*(s)分布结果;(f)Milk-EXODUS的A260/A280比值。
基于以上研究发现,单一技术不足以全面表征外泌体。DLS技术适用于样品的快速初筛;NTA技术是分析外泌体粒径分布与动态变化的核心手段;NanoCoulter技术可在特定粒径范围内提供准确的浓度和粒径数据;而AUC技术则在外泌体纯度评估方面具有重要的应用潜力。将AUC与NTA、NanoCoulter等方法进行正交验证,有望建立更标准化、可重复的外泌体质量控制体系。
该研究为外泌体作为药物载体的质量评价提供了全新的技术策略,也彰显了AUC技术在复杂生物纳米颗粒表征中的广阔应用前景。
三.总结
通过这两项研究成果的系统整合,可以清晰看到AUC技术在生物医药质量控制中的巨大应用潜力。AUC技术不再仅仅是一项用于测定沉降系数的经典技术,而是一项能够提供分子量、组分比例、异质性、纯度及光学特性等多维度信息的表征工具。
无论是结构复杂的糖蛋白、质控严格的结合疫苗,还是高度异质的外泌体,AUC技术均能展现出独特的应用优势。AUC技术可在天然状态下提供“绝对”定量的数据,为其他快速、高通量的方法提供了可靠的校准依据和数据补充。
随着 AUCAgent 国产化高易用性分析软件的出现,AUC技术的应用门槛也将进一步降低。在生物药的质量控制、新型疫苗的研发以及纳米药物的表征等领域,AUC技术将发挥越来越关键的支撑作用。
清华大学蛋白质研究技术中心/生物结构前沿研究中心王朝兴为共同第一作者。清华大学蛋白质研究技术中心/生物结构前沿研究中心/膜生物学国家重点实验室李文奇为共同通讯作者。
原文链接
https://doi.org/10.3390/ph19020210
https://doi.org/10.1038/s41598-026-46079-8